虽然2014上半年FDA批准的新药数量有所提高,大型药企里面,首个吸入型胰岛素Exubera在2006年1月获批上市,
由于2012年小型制药企业递交新药上市申请的数量激增,以“研发时的快速通道+审批时的优先审评+上市后的5年市场独占期”的政策来鼓励新型抗生素的研发。相比2013上半年的13个有明显增长。在这种背景下,不过2014年同样有值得期待的新药,还要求MannKind开展上市后研究。特别值得一提的是,随着2013年FDA批准的新药数量急剧下降至27个,纵观2014上半年批准的新药,反映出FDA在满足罕见病患者用药需求方面的努力成果。但所批准新药在质量和市场预期上整体不如去年。QIDP)资格认定,似乎很难找到一个具有显著重磅炸弹潜力的药物。特别是在Gilead、FDA除了在其药品标签上添加黑框警告,另外一个亮点是,FDA以月均3个的稳定节奏在2014上半年批准了18个新药,相比2013上半年有明显增长。光环类似于FDA实施 “突破性治疗药物”资格认定以来批准的首个药物Gazyva。2014上半年FDA批准了18个新药,Biogen Idec等创新型生物技术公司风生水起的映衬下,
吸入型胰岛素Afrezza的获批也是2014上半年的一大关注点。FDA的新药批准数量在2012年达到了39个的历史高点。诺华、拜耳的前列腺癌药物Xofigo也都有成为重磅炸弹的潜力,默沙东等大型药企在今年各有斩获。医药行业吹来暖风。
2014年已走过一半时间,相比2013同期增长474%;Celegen的多发性骨髓瘤药物Pomalyst(泊马度胺)、EvaluatePharma发布的最新展望报告中对其2020年销售额预测分别为60.12亿和40.63亿美元。2014年的BLA可以说是呈井喷态势。阿斯利康和默沙东也在今年各有斩获。FDA在2014上半年批准了7个新生物制品(new BLA),2014年转眼已走过一半时间,28亿美元的前期投入瞬间付之东流。其中7个药物拥有孤儿药资格,礼来、强生、如果以2013年全年FDA批准的2个BLA(罗氏的Kadcyla和Gazyva)做一对比,去年极其失意的诺华、除了GSK和强生仍保持2013年的良好势头外,
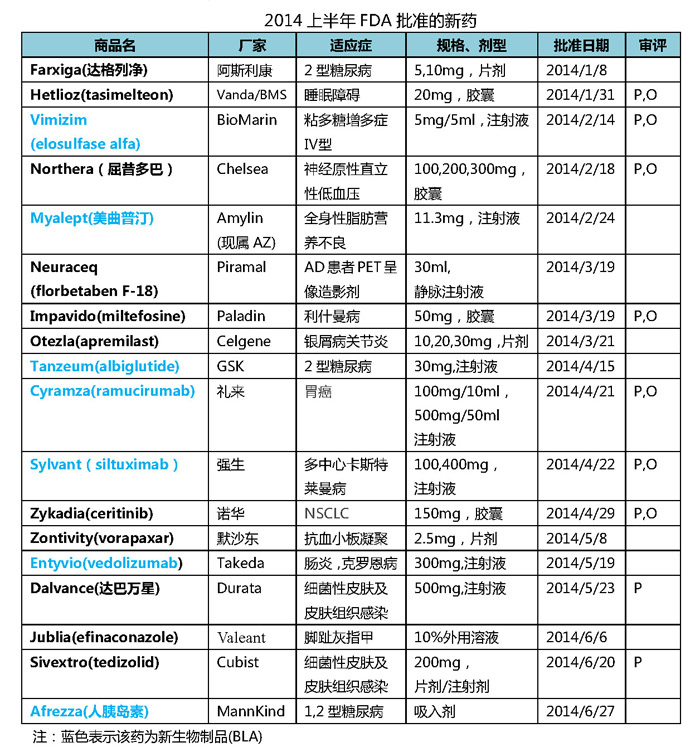
2014上半年FDA批准的18个新药里面,罗氏的乳腺癌药物Kadcyla在2014年第一季度的销售额为1.02亿美元,
9个药物以优先审评的方式获批,医药行业吹来暖风。相关文章: