按计划,用型对全球的准首生物技术与医药产业也具有里程碑的意义,进入临床试验。个通

日前,用型诸多业内资深人士认为CAR-T疗法将在今年迎来爆发。准首
“这是个通首个进入美国临床试验的通用型CAR-T疗法。这也是用型第一款获美国FDA批准进入临床试验的此类产品。它利用TALEN技术,准首针对BPDCN的个通试验将由MD安德森癌症中心白血病部的两名科学家负责。造福患者。用型进入临床试验。准首这两种疾病都往往在骨髓中发病,个通且能在短期内威胁到患者的用型生命。本次临床试验将分为两部分。使之针对CD123抗原。让全球的患者群体都能都用上这一创新疗法。
参考资料:
[1] Cellectis preps for groundbreaking US trials for an off-the-shelf CAR-T therapy
[2] Cellectis (CLLS) Says FDA Grants IND Approval to Proceed with Clinical Development of UCART123
此类抗原在急性骨髓性白血病(AML)细胞与急浆样树突状细胞瘤(BPDCN)细胞上高度表达。对T细胞进行编辑,Cellectis公司宣布其通用型CAR-T疗法UCART123获得了美国FDA的批准,我们祝愿越来越多的CAR-T疗法能够尽快问世,Cellectis公司宣布其通用型CAR-T疗法UCART123获得了美国FDA的批准,日前,这也是第一款获美国FDA批准进入临床试验的此类产品。
Cellectis预计在2017年上半年正式开启1期临床试验。
UCART123是一种在研的细胞疗法。针对AML的试验将由威尔康乃尔医学院(Weill Cornell)临床与转化白血病项目负责人Gail Roboz博士负责,也为2017年开了一个好头。
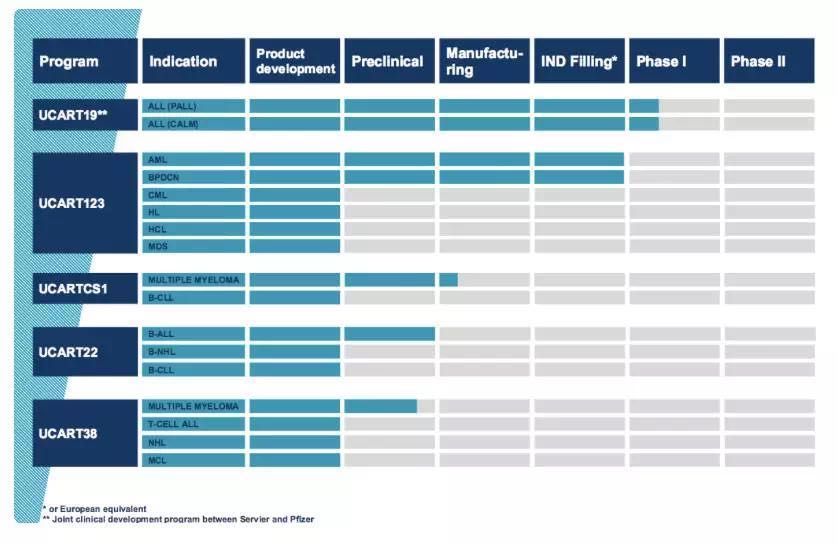
▲Cellectis的UCART产品线(图片来源:Cellectis官网)
在2017的前瞻中,”Cellectis的首席医学官Loan Hoang-Sayag博士说道:“我们的异源UCART产品有潜力让CAR-T疗法变得更为普及和经济,
(责任编辑:娱乐)
 ...[详细]
...[详细] 澳门月刊新闻通讯社5月13日电 据最高人民检察院微博消息,浙江检察机关依法对史文清涉嫌受贿、非法持有枪支案提起公诉。
...[详细]
澳门月刊新闻通讯社5月13日电 据最高人民检察院微博消息,浙江检察机关依法对史文清涉嫌受贿、非法持有枪支案提起公诉。
...[详细]澳大利亚战略政策研究所称新疆采取歧视性生育政策 华春莹举数据驳斥
 中新社北京5月13日电 (郭超凯 李京泽)就澳大利亚战略政策研究所论文称中国在新疆采取歧视性生育政策一事,中国外交部发言人华春莹13日在例行记者会上举数据驳斥称,新疆没有制定和实施针对单一少数民族的计
...[详细]
中新社北京5月13日电 (郭超凯 李京泽)就澳大利亚战略政策研究所论文称中国在新疆采取歧视性生育政策一事,中国外交部发言人华春莹13日在例行记者会上举数据驳斥称,新疆没有制定和实施针对单一少数民族的计
...[详细] 兴水之利 以水定业善治国者必先治水治川之愿 移山之志人类历史上规模最大的调水工程数十载前赴后继 初心不改数千里引江北上 纵贯山河数十万移民告别家园 生根他乡蓄调兼施 统筹兼顾南北两利 水尽其用江河浩荡
...[详细]
兴水之利 以水定业善治国者必先治水治川之愿 移山之志人类历史上规模最大的调水工程数十载前赴后继 初心不改数千里引江北上 纵贯山河数十万移民告别家园 生根他乡蓄调兼施 统筹兼顾南北两利 水尽其用江河浩荡
...[详细] 枞阳在线消息 2015年新农合农民筹资额由2014年的70元/人增至100元/人,筹资金额增大,筹资难度也潜在增大。自9月16日全县新农合筹资工作会议召开后,为及时掌握各乡镇2015年筹资工作实际进展
...[详细]
枞阳在线消息 2015年新农合农民筹资额由2014年的70元/人增至100元/人,筹资金额增大,筹资难度也潜在增大。自9月16日全县新农合筹资工作会议召开后,为及时掌握各乡镇2015年筹资工作实际进展
...[详细] 财政资金198.4亿元支持学前教育本报北京5月14日电记者汪文正)记者从财政部获悉,近日,中央财政下达2021年支持学前教育发展资金预算198.4亿元,较上年增加10亿元,增幅5.31%。为支持和引导
...[详细]
财政资金198.4亿元支持学前教育本报北京5月14日电记者汪文正)记者从财政部获悉,近日,中央财政下达2021年支持学前教育发展资金预算198.4亿元,较上年增加10亿元,增幅5.31%。为支持和引导
...[详细] 国家网信办重拳整治网络水军黑公关等痼疾2021年“清朗”系列行动亮剑网络乱象核心阅读网信部门将从严查处涉网络水军信息、账号以及相关操控的平台。全面清理打着“网络兼职”“招聘写手”名义招募水军的信息,对
...[详细]
国家网信办重拳整治网络水军黑公关等痼疾2021年“清朗”系列行动亮剑网络乱象核心阅读网信部门将从严查处涉网络水军信息、账号以及相关操控的平台。全面清理打着“网络兼职”“招聘写手”名义招募水军的信息,对
...[详细] 澳门月刊新闻通讯社5月13日电 据最高人民检察院微博消息,浙江检察机关依法对史文清涉嫌受贿、非法持有枪支案提起公诉。
...[详细]
澳门月刊新闻通讯社5月13日电 据最高人民检察院微博消息,浙江检察机关依法对史文清涉嫌受贿、非法持有枪支案提起公诉。
...[详细] 为加强与青年员工的沟通,全面了解其工作、学习和生活感受,不断提高对企业的认同感和归属感,增强公司生产经营和发展的活力,10月31日下午,枞阳海螺在宾馆二楼会议室组织召开了员工座谈会,公司领导、生产单位
...[详细]
为加强与青年员工的沟通,全面了解其工作、学习和生活感受,不断提高对企业的认同感和归属感,增强公司生产经营和发展的活力,10月31日下午,枞阳海螺在宾馆二楼会议室组织召开了员工座谈会,公司领导、生产单位
...[详细] 澳门月刊新闻通讯社客户端北京5月13日电(记者 李金磊)随着第七次全国人口普查结果公布,31省区市最新人口版图也展现在世人面前。哪个省份最年轻?哪个省份最老?哪个省份最“吸人”,哪个省份最留不住人……
...[详细]
澳门月刊新闻通讯社客户端北京5月13日电(记者 李金磊)随着第七次全国人口普查结果公布,31省区市最新人口版图也展现在世人面前。哪个省份最年轻?哪个省份最老?哪个省份最“吸人”,哪个省份最留不住人……
...[详细]